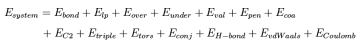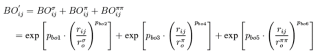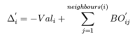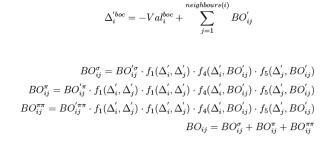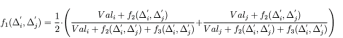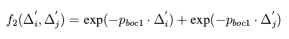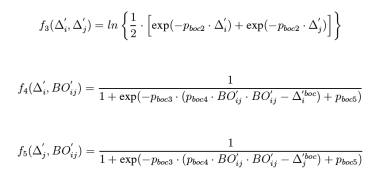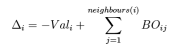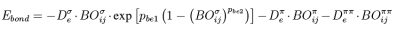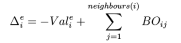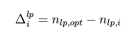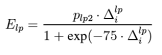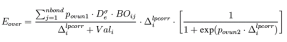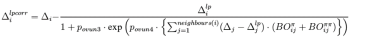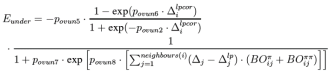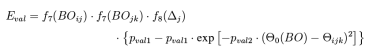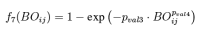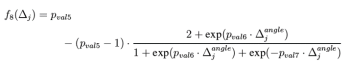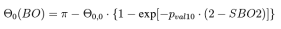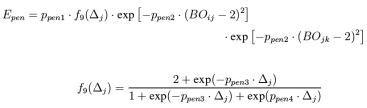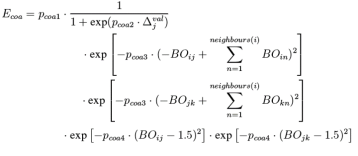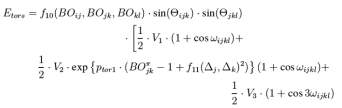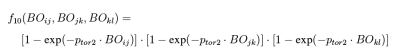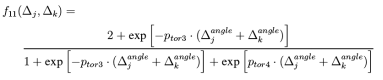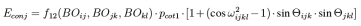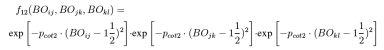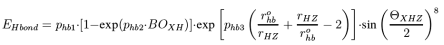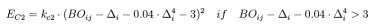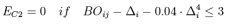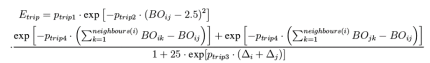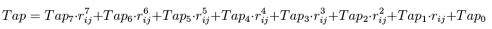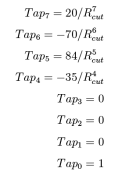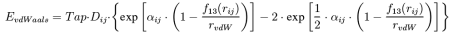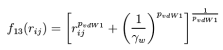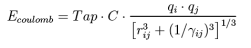|
LAMMPS讲解68-ReaxFF力场公式介绍在常用的分子动力学中,化学键是不能被打断和形成,因此无法模拟化学反应。为克服这一缺陷,研究者提出了反应分子动力学模拟方法。在反应分子动力学中最重要的就是采用反应力场。在经典力场中如OPLSAA,AMBER等,同一种元素的原子根据所处化学环境的不同会具有不同的类型。与经典力场不同,在反应力场中不存在原子类型,同一个分子内的原子没有用固定的化学键直接相连,而是通过计算任两个原子之间的键级来确定当前时刻的连接性。在反应分子动力学模拟过程中,随着键级的变化,化学键会不断的断裂和生成,而原子之间的连接列表即成键性也在不断的更新。因此在反应力场中键级是最重要的量,在键级的基础上将原子之间的相互作用表达为键级的函数,由此计算出经典力场中的键,键角,二面角,共轭,库伦,范德华等相互作用。对于反应力场,系统中的总能量表示为:
键能:在键级的定义中一个基本假设就是键级和原子之间的距离成特定的数学关系,通过原子之间的距离可以之间计算出键级的大小。在反应力场中根据原子之间的距离的不同将化学键分为单间,双键和三键。一个原子的键级来自三种键的加和贡献:
直接计算的键级是未经校正过的键级,需要对键级进行校正。在此之前首先要定义过配位数
上式中的过配位数也是未经过校正的,式中Vali是原子i的总键级,例如C原子的总键级是4,氢原子的总键级是1。在未经校正的键级和过配位数的基础上,反应力场通过下式对过配位数进行,为使得校正不至于太硬,引入了第二过配位数,即
经过校正就可以得到新的键级,同时新的过配位数由下式得到
由此任一个键的键能由下式得到:
孤对电子能:在某些体系中存在孤对电子,而孤对电子对体系的结构和能量也有着较大的影响。反应力场中为了能够处理这样的体系引入了下述两个函数来表达原子外层孤对电子对系统能量的贡献:
其中nlp,i为原子外层的孤对电子数,Valie为原子的最外层电子数。在原子的键级发生变化时,孤对电子的变化为:
此时孤对电子对体系能量的贡献为:
过配位的能量校正项:当原子的过配位数大于零是,由键级得到体系能量需要进行校正,同时考虑孤对电子的存在的校正分别为:
过配位能量校正项:当过配位数小于零时,同样需要对体系的能量进行校正,但是这种校正只有存在π键时才执行
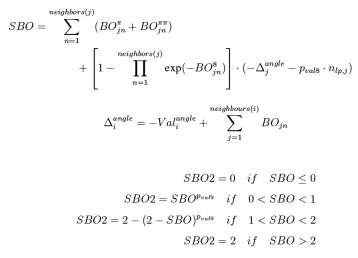
键角能量项:与键能量项类似,在反应力场中键角的能量也表示为键级的函数,键角能量的计算通过下式来完成,其中平衡键角取决于π键键级总和的函数SBO,通过条件判断,可以硅键角中心原子的杂化状态进行判断:
为处理键角中心原子两边各连两个双键的情况,反应力场中加入了键角能量惩罚项:
在一般的共轭体系中,反应力场的对四体共轭项也能合理的处理,但是在处理特定基团的共轭时会出现问题,为此引入三体共轭项:
四体作用项:与键角类似,在处理二面角时需要确定四个相连原子的键级数,因此在反应力场中四体作用项描述为:
对于四体作用中的共轭情况,采用四体共轭项进行描述:
氢键作用项:
C2修正项:在反应力场中对于两个C原子分子当存在三键时,这个三键的能量要远远高于CC双键,但是,实际上三键会很大程度上被末端的自由基削弱,是的这个三键的能量低于双键。为对这种情况进行修正,反应力场引入了新的能量修正项:
三键修正项:为对一氧化碳分子的碳氧三键进行修正引入:
范德华相互作用项:除了电子云重叠而出现的键结能量外,体系中原子还存在着非键结相互作用,其中一项就是范德华相互作用。这部分能量的计算与经典分子动力学相似,所不同的是当原子跨越截断半径的时候能量会出现不连续现象,为避免这种现象的出现特引入Taper函数:
这个七阶的多项式能够保证非键结相互作用具有一阶,二阶和三阶导数连续性同时可保证在截断半径位置出的相互作用能量连续趋于零,各项的数学表达式如下:
在范德华相互作用中采用Morse函数形式,同时为避免键结的两个原子与相间的两个原子之间出现过高的排斥作用引入近程修正项:
库伦相互作用:在计算库伦相互作用是采用QEq方法,即通过原子间的距离变化计算瞬时的原子电荷,以满足反应力场的化学键断裂和生成的要求:
感谢鲍路瑶老师的分享,内容来自于鲍老师分享出来的资料 如有需要添加微信:lmp_zhushou 进入微信群,帮助他人,共建社区 获取完整版lammps讲义可以加微信lmp_zhushou或加入QQ群994359511 |